Em. 1865, o químico inglês J.A.R. Newlands organizou os elementos químicos em ordem crescente de massa atômica e colocou-os em colunas verticais. Cada uma das colunas verticais possuía sete elementos. O modelo era chamado Lei das oitavas.
Em 1869, Dmitri Ivanovich Mendeleev (1834-1907) organizou os elementos químicos em filas horizontais em ordem crescente de massa atômica e mostrou que nas linhas verticais havia elementos com propriedades químicas e físicas semelhantes. Com isso, foi considerado o pai da Tabela Periódica.
O trabalho do homem foi tão incrível que ele conseguiu relacionar as propriedades periódicas, as quais se repetiam em intervalos regulares, dos elementos. E, além disso, conseguiu até mesmo prever a existência de determinados elementos que ainda não haviam sido descobertos, onde eles ficariam na Tabela Periódica e quais seriam as suas propriedades.
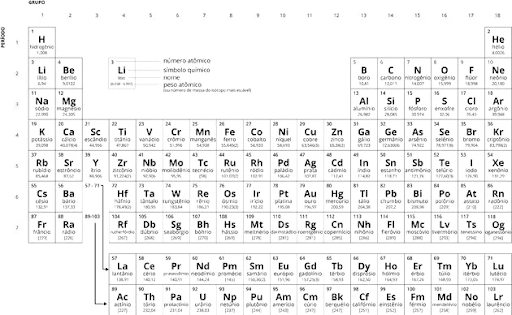
Em 1913, o físico inglês Henry Moseley, fez um experimento com raios X e descobriu o número atômico (Z) dos elementos químicos e definiu que a quantidade de prótons que há no núcleo dos átomos de cada elemento. Ele provou que as propriedades dos elementos tinham relação não com a massa atômica, como dizia Mendeleev, mas sim com o número atômico. Manteve a organização em colunas horizontais e verticais, mas posicionou os elementos de mesmas características químicas nas mesmas colunas verticais.
Atualmente, A última atualização da Tabela Periódica aconteceu em 2016 quando os elementos 113, 115, 117 e 118 passaram a fazer parte oficialmente dela.
Hoje em dia, a tabela é organizada em colunas – grupos ou famílias – e linhas – períodos.
GRUPOS OU FAMÍLIA:
Esse nome faz mito sentido. Imagina aí um ambiente familiar (às vezes é melhor não, so choro), os membros de uma família possuem várias características físicas, emocionais e psicológicas parecidas, além disso, os membros de um grupo específico possuem, também, vontades e gostos similares.
Analogicamente, isso acontece com os elementos de um mesmo grupo da tabela: os elementos pertencentes a um mesmo grupo ou a uma mesma família da Tabela Periódica possuem propriedades físicas e químicas semelhantes.
Isso acontece, porque elementos de um mesmo grupo da tabela possuem a memsa quantidade de elétrons na camada de valência, ou seja, a última camada.
Alguns grupos recebem “apelidos”, um tipo de nome especial. São eles:
Família 1: Metais alcalinos;
Família 2: Metais alcalinoterrosos;
Família 16: Calcogênios;
Família 17: Halogênios;
Família 18: Gases Nobres.
Ainda nessa parte, a tabela tambem possui subgrupos. São eles:
Elementos representativos: todos os elementos representativos possuem o seu elétron mais energético situado nos subníveis “s” ou “p”.
Elementos de transição: todos os elementos de transição possuem o seu elétron mais energético situado nos subníveis “d” ou “f”.
- Elementos de transição externa: Eles estão representados na região central da Tabela. Seus elétrons mais energéticos ficam no subnível “d”.
- – Elementos de transição interna: série dos lantanídeos e a série dos actinídeos. Seus elétrons mais energéticos ficam no subnível “f”. Seu grupo é o 3 ou família III B.
Ps: a IUPAC, atualmente, adota a nomenclatura GRUPO ao invés de família.
PERÍODOS OU LINHAS:
as linhas horizontais são os períodos e indicam a quantidade de níveis eletrônicos, ou seja, de camadas eletrônicas que os átomos possuem. A eletrosfera possui 7 níveis, os quais representam as 7 linhas da tabela.
É HORA DE TREINAR!!!
1. (UFU) No início do século XIX, com a descoberta e o isolamento de diversos elementos químicos, tornou-se necessário classificá-los racionalmente, para a realização de estudos sistemáticos. Muitas contribuições foram somadas até se chegar à atual classificação periódica dos elementos químicos. Em relação à classificação periódica atual, responda:
a) Como os elementos são listados, sequencialmente, na tabela periódica?
b) Em quais grupos da tabela periódica podem ser encontrados: um halogênio, um metal alcalino, um metal alcalinoterroso, um calcogênio e um gás nobre?
2. (Unitins) Com relação à classificação periódica moderna dos elementos, identifique a afirmação verdadeira:
a) em uma família, os elementos apresentam geralmente o mesmo número de elétrons na última camada.
b) na tabela periódica, os elementos químicos estão colocados em ordem decrescente de massas atômicas.
c) em uma família, os elementos apresentam propriedades químicas bem distintas.
d) em um período, os elementos apresentam propriedades químicas semelhantes.
e) todos os elementos representativos pertencem ao grupo B da tabela periódica.
3. (F. Ibero-Americana-SP) O grupo da Tabela Periódica que se caracteriza por apresentar predominância de elementos artificiais é o dos:
a) lantanídios
b) gases nobres
c) metais de transição
d) metais alcalinoterrosos
e) actinídios
4. (Uel)
Considere os itens a seguir. Na tabela periódica
I. os elementos representativos são os das famílias indicadas com letras A (1A, 2A etc…).
II. Na, Mg, Ca, Rb, Ba e Ra são os elementos alcalinos.
III. F, O e Cl estão entre os elementos mais eletronegativos.
Pode-se afirmar que, SOMENTE
a) I é correto.
b) II é correto.
c) III é correto.
d) I e II são corretos.
e) I e III são corretos.
5. (UFC – CE) Com relação à classificação periódica moderna dos elementos, assinale a afirmação verdadeira:
a) Na Tabela Periódica, os elementos químicos estão colocados em ordem decrescente de massas atômicas.
b) Em uma família, os elementos apresentam propriedades químicas bem distintas.
c) Em uma família, os elementos apresentam geralmente o mesmo número de elétrons na última camada.
d) Em um período, os elementos apresentam propriedades químicas semelhantes.
e) Todos os elementos representativos pertencem aos grupos B da tabela periódica.
GABARITO:
2. A; 3. E; 4. E; 5. C